Indicazioni per la chirurgia della cataratta nei bambini
La cataratta congenita può causare deficit visivi nei bambini[1]. È causa di circa il 10% dei casi di cecità infantile in ambito mondiale[2]. In particolare una porzione rilevante di casi si verifica nei paesi in via di sviluppo[3,4].
A causa del rapido sviluppo della visione nei primi 4 mesi di vita (sviluppo del riflesso di fissazione), una mancanza o limitazione delle sensazioni visive dovuta ad un cristallino opaco determina nella maggior parte dei casi ambliopia, strabismo, nistagmo o addirittura una diminuzione secondaria di neuroni nei corpi genicolati laterali e nella corteccia visiva (VDS – Visual Deprivation Syndrome).
Le cause della cataratta congenita sono innumerevoli; in particolare sono da segnalare i fattori genetici, le infezioni intrauterine, l’utilizzo di farmaci durante la gravidanza e i disordini metabolici nei bambini[1]. La gestione clinica dipende in modo primario dalla natura e dalla gravità della cataratta. L’ambliopia, le difficoltà intra- e post-operatorie, i frequenti controlli medici fanno del trattamento della cataratta congenita una sfida impegnativa.
Tutte queste problematiche rendono la chirurgia della cataratta nei bambini tecnicamente più complessa che negli adulti.
Indicazioni per la chirurgia della cataratta nei bambini
La principale indicazione per la rimozione della cataratta è l’opacizzazione del cristallino che impedisce il normale sviluppo visivo.
Quando operare la cataratta nei bambini?
È opinione condivisa che il massimo decremento dell’acuità visiva si determini nelle prime settimane di vita. Fino alle 14 settimane di età, ogni tre settimane di ritardo nell’effettuare l’intervento causano una riduzione dell’acuità visiva di una linea nelle tavole di Snellen. Tra le 14 e le 31 settimane di età si ha un ulteriore lieve decremento dell’acuità visiva. La chirurgia della cataratta effettuata entro le 4 settimane di età riduce l’incidenza di strabismo e nistagmo[5].
Si ritiene che le cataratte unilaterali debbano essere operate prima della sesta-ottava settimana, e la cataratta bilaterale prima della decima settimana di età[6,7]. A causa del rischio di ambliopia, il trattamento chirurgico dovrebbe essere effettuato quanto prima possibile. Tuttavia in letteratura è riportata una maggiore incidenza di glaucoma secondario se il trattamento chirurgico viene effettuato troppo presto[5,7,8].
Biometria e calcolo del potere della lente intraoculare
La significativa crescita dell’occhio nei primi anni di vita del bambino e le difficoltà nel prevedere la lunghezza finale del bulbo oculare sono la causa principale dei problemi di calcolo del potere delle lenti intraoculari. I cambiamenti refrattivi sono il risultato della crescente lunghezza assiale del bulbo oculare, che varia da 16,8 mm nel neonato a 22,6 mm nell’adulto, e del cambiamento nella curvatura della cornea (51,2 D nel neonato; 43,5 D nell’adulto) e della lente (34,4 D nel neonato; 18,8 D nell’adulto).
Ciò fa sì che la maggior parte dei chirurghi preferiscano ipocorreggere i bambini piccoli al momento della chirurgia (puntando a una correzione ipermetropica), in previsione di una significativa variazione miopica nel tempo. Enyedi et al hanno proposto delle linee guida per l’individuazione degli obiettivi refrattivi alle diverse età in base ai dati del loro studio, come illustrato nella Tabella I[9].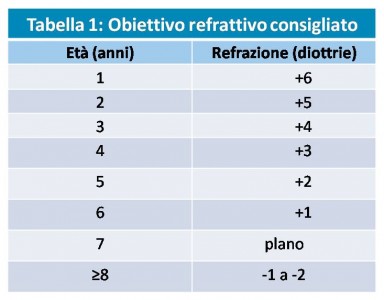
Non è emersa, in base ai dati di diversi studi, una maggiore efficacia di una delle formule utilizzate nel calcolo del potere delle lenti intraoculari. Di solito vengono applicate SRK II, SRK / T, Hoffer Q e Holladay[10]. Dahan et al suggeriscono di lasciare nei bambini al di sotto dei due anni di età un 20% di ipocorrezione e un 10% nei bambini di 2-8 anni[11]. Lu et al riducono il potere dell’impianto di un 30% nei bambini di 6-12 mesi. Dopo la chirurgia, tutti i bambini dovrebbero essere corretti con occhiali o lenti a contatto[12].
La scelta della lente intraoculare (IOL)
La scelta della IOL e l’età del bambino al momento dell’impianto sono oggetto di controversia.
Si deve ricordare che minore è l’età del paziente al momento dell’impianto della IOL, maggiore è il rischio di re-intervento per via di complicanze[13]. Le lenti intraoculari artificiali vengono di solito impiantate in bambini di più di 2 anni (nel primo anno di vita la refrazione cambia di circa 10 D).
Nella letteratura attualmente disponibile, l’età minima dei pazienti chirurgici per impianto di IOL è 7 giorni[14]. LU et al sostengono che gli impianti di lenti intraoculari sono sicuri nei bambini tra i 6 e i 12 mesi di età[12].
Il sito più ampiamente utilizzato per l’impianto della IOL è il sacco capsulare. Esso assicura il sequestro della IOL dal tessuto vascolarizzato. La fissazione della IOL nel solco ciliare crea maggiori problemi, in quanto la lente entra a contatto con la coroide. Alcuni oculisti pediatrici affermano che l’inserimento della lente intraoculare nel sacco per gli occhi afachici è ideale, ma si tratta di una tecnica molto difficile[15].
In precedenti osservazioni si sono ottenuti risultati molto buoni con l’impianto di lenti in acrilico idrofilo[3,16]. L’AAPOS (American Association for Pediatric Ophthalmology and Strabismus) raccomanda la lente monopezzo AcrySoft per l’impianto nei bambini. È facile da impiantare ed è sicura anche in neonati e bambini con macroftalmia. L’impianto di lenti in acrilico idrofobo è associato ad un minore rischio di opacizzazione della capsula posteriore e di glaucoma secondario[3]. Sulla superficie delle lenti in acrilico idrofilo sono stati osservati depositi di calcio e fosfato in un breve periodo dopo il trattamento chirurgico[17,18]. Anche le lenti in silicone accelerano lo sviluppo di depositi di calcio e sono spesso associate ad un rischio più elevato di fimosi capsulare posteriore[19]. Le lenti multifocali non sono consigliate per l’impianto nei bambini, in quanto richiedono una biometria precisa e una perfetta centrazione, che possono variare durante il periodo di guarigione, per eventuale fibrosi e crescita dell’occhio. Negli ultimi anni sono stati pubblicati alcuni studi in cui gli autori descrivono l’utilizzo nei bambini di IOL a supporto irideo. Sminia et al. hanno impiantato la lente Artisan in 10 bambini dell’età media di 7,4 anni negli anni 1991-1999. La densità media delle cellule corneali endoteliali (ECD) era 2.702 cellule/mm² 12 anni dopo il trattamento chirurgico, ed era comparabile alla ECD media normale per quel gruppo d’età, come riportato in letteratura[20].
Difficoltà dell’intervento di cataratta nei bambini
La chirurgia della cataratta nei bambini è tecnicamente più complessa che negli adulti. Ciò è dovuto all’anatomia dell’occhio del bambino. Il cristallino è piccolo, la camera anteriore è poco profonda, la capsula anteriore è molto elastica e spessa, la capsula posteriore è 3-5 volte più sottile e meno elastica che negli adulti. Inoltre, una bassa rigidità sclerale rende difficile realizzare incisioni auto-sigillanti. Le difficoltà nella midriasi spesso richiedono l’utilizzo dei retrattori iridei. Nel corso del trattamento chirurgico si osserva spesso un’accresciuta pressione vitreale, in genere come risultato di una subsidenza sclerale, che determina una riduzione di profondità della camera anteriore ed un prolasso irideo. A causa dell’incremento della pressione vitreale, la IOL tende a “distorcersi” dal sacco capsulare, invece di restare collocata nel suo interno.
Inoltre le complicanze postoperatorie, sia precoci che tardive, si verificano più frequentemente che negli adulti. Reazioni infiammatorie molto intense, fibrosi e una rapida opacizzazione della capsula posteriore richiedono una particolare gestione intra- e postoperatoria.
Tecnica chirurgica
Le problematiche operatorie più frequenti nella chirurgia della cataratta pediatrica sono: la gestione della capsula anteriore e posteriore, e l’effettuazione della vitrectomia anteriore. L’accesso chirurgico è in genere attraverso la cornea o la pars plana. L’ampiezza media in pars plana varia da 1,5 – 2 mm nei neonati, a 3 mm a 6 mesi di età.
La capsuloressi manuale anteriore curvilineare continua, con un margine il più regolare possibile, costituisce il “gold standard” per un risultato di successo nella chirurgia della cataratta pediatrica. È la scelta privilegiata dai chirurghi per pazienti di due o più anni di età. La vitrectoressi viene preferita dai chirurghi durante i primi due anni di vita. La capsulotomia anteriore può essere effettuata utilizzando l’endodiatermia a radiofrequenza, ma la dimensione finale sarà maggiore.
L’opacizzazione posteriore della capsula (PCO) è il risultato della proliferazione, migrazione e metaplasia delle cellule epiteliali derivanti dalla regione equatoriale della capsula anteriore alla capsula posteriore. Quando la capsula posteriore viene lasciata intatta nel corso dell’intervento, l’incidenza di PCO è del 100%. L’insorgenza di PCO aumenta in genere 18 mesi dopo la chirurgia. Pertanto, in bambini con meno di 8 anni di età la capsulotomia posteriore dovrebbe essere effettuata con una vitrectomia anteriore addizionale[21]. Wilson lascia intatta la capsula posteriore nei bambini con più di 6 anni di età. Nei bambini piccoli effettua una capsulotomia posteriore via pars plana: nei neonati a 0,5 mm posteriormente al limbus, sotto un anno di età a – 2 mm posteriormente al limbus, sotto i 4 anni a – 2,5 mm posteriormente al limbus[3].
Quando il corpo vitreo viene inciso dal retro, si determina un minore rischio di distacco della retina e di edema maculare cistoide.
La gestione della capsula posteriore nei bambini con cataratta congenita, raccomandata da Vasavada, è schematizzata nella Tabella II[24].
Complicanze dopo la chirurgia
La complicanza più comune dopo la chirurgia della cataratta congenita è il glaucoma secondario. La sua prevalenza è del 15,4 – 19,5% entro i 10 anni successivi alla chirurgia[1,2]. Sono, quindi, molto importanti, controlli medici regolari da effettuare per molti anni dopo l’intervento.
Un’età inferiore ai 9 mesi al momento della chirurgia ed una micro-cornea predispongono allo sviluppo di glaucoma secondario[2]. Nei bambini operati prima dei 9 mesi di età, il glaucoma insorge 3,8 volte più spesso che nei bambini operati dopo questa età[2,23]. PHPV (Persistent Hyperplastic Primary Vitreous), una capsulotomia posteriore primaria o una vitrectomia non predispongono allo sviluppo di glaucoma secondario[2]. Nei pazienti con glaucoma, la cataratta bilaterale è risultata leggermente più frequente delle opacizzazioni unilaterali del cristallino[2]. L’intervallo di tempo medio per l’insorgenza del glaucoma dopo l’intervento chirurgico per una cataratta congenita variava da alcune settimane a molti anni[2,8,23].
Raramente è stato riportato il distacco di retina nei bambini a seguito della chirurgia della cataratta congenita[13]. La complicanza postoperatoria meno comune è l’uveite fibrinosa[4].
In letteratura si possono leggere report di accresciuta miopia nei bambini, specialmente nei primi 2 anni dopo la chirurgia[12,14].
In sintesi
Il successo nel trattamento della cataratta congenita dipende in primo luogo da una diagnosi precoce della patologia. La riuscita del trattamento è connessa alla scelta del tempo chirurgico ottimale, alla precoce riabilitazione visiva e ad una buona collaborazione con i genitori. Realizzare tutte queste condizioni consente di garantire un’adeguata acuità visiva, da cui dipenderà la funzione visiva in età adulta.
Alina Bakunowicz-?azarczyk, Beata Urban, Anna Bryl
Department of Pediatric Ophthalmology MU in Bialystok, Poland
Per eventuali quesiti – e-mail: alina.lazarczyk@umb.edu.pl
CONTROVERSIES IN PEDIATRIC CATARACT MANAGEMENT
(testo originale in lingua inglese)
Congenital cataract may cause visual impairment in children[1]. It constitutes approximately 10% of blindness cases among children, globally[2]. In particular, a large proportion of cases occurs in developing countries[3,4]. Due to the rapid development of vision in the first 4 months of life (developing fixation reflex), lack or limitation of visual sensations by the cloudy lens most often results in amblyopia, strabismus, nystagmus or even a secondary reduction of neurons in the lateral geniculate bodies and visual cortex (VDS – Visual Deprivation Syndrome).
There are many causes of congenital cataract; genetic factors, intrauterine infections, drugs used during pregnancy and metabolic disorders in children are specially emphasised[1]. The procedure primarily depends on the nature and severity of the cataract. Amblyopia, intra- and postoperative difficulties, frequent medical visits make that treatment of congenital cataract a challenge. All these dilemmas make cataract surgery in children technically more difficult than in adults.
Indications forcataract surgery in children
The main indication for cataract removal is cloudiness in the lens preventing normal visual development.
When to operate cataract in children?
It is believed that the greatest decrease in visual acuity falls on the first weeks of life. Up to 14 weeks of age, every three weeks delay in treatment causes a decrease in visual acuity of one line on the Snellen chart. Between 14 and 31 weeks of age is a further slight decrease in visual acuity. Cataract surgery to 4 weeks of age reduces the incidence of strabismus and nystagmus[5]. It is believed that the unilateral cataracts should be operated before the 6-8th week, and bilateral cataract before the 10th week of age[6,7]. Due to the risk of amblyopia, surgery should be performed as soon as possible. However, in the available literature a higher incidence of secondary glaucoma is described, if the treatment is carried out too early[5,7,8].
Biometry and intraocular lens power calculation
The significant growth of the eye in the first years of a child’s life and difficulties in predicting the final length of the eyeball, are the main cause of problems with the intraocular lens power calculation. Refractive changes are the result of increasing axial length of the eyeball, which varies from 16.8 mm in newborn to 22,6 mm in adult and a change in curvature of the cornea (51.2 D in newborn; 43.5 D in adults) and the lens (34.4 D in newborn; 18.8 D in adults).
It makes most surgeons prefer undercorrecting young children at the time of surgery (targeting for a hyperopic correction) in anticipation of a significant myopia shift over time. Enyedi et al presented guidelines for target refractions for various ages based on the results of their study. They are shown in Table I[9].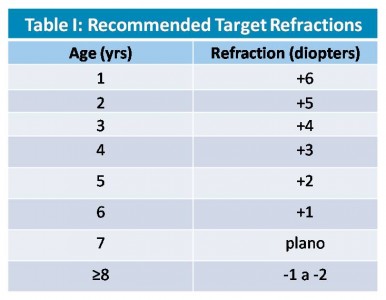
Many studies have not shown greater efficacy of one of the formulas used in the calculation of intraocular lenses in children. SRK II, SRK / T, Hoffer Q and Holladay are usually used [10]. Dahan et al suggest leaving in children under two years of age 20% hypocorrection and 10% in children aged 2-8 years[11]. Lu et al reduce the power of the implant by 30% in children aged 6-12 months. After surgery, all children should be corrected with glasses or contact lenses[12].
Choosingan intraocular lens (IOL)
IOL selection and age of child during IOL implantion are controversial. It must be remembered, that the younger age of the patient with implanted lens, the higher risk of reoperation due to complications[13]. Artificial intraocular lenses used to be implanted in children over 2 years (in the first year of life refraction changes are about 10 D). In the available literature, the minimum age for surgical patients with an intraocular lens is seven days[14]. LU et al suggest, that intraocular lens implants are safe in children between 6 and 12 months of age[12]. The most popular site for IOL implantation is capsular bag. It provides IOL sequestration of vascularized tissue. Ciliary sulcus fixation of IOL is worse, because lens is in contact with the choroid. Some pediatric ophthalmologists recognize that In-the-bag intraocular lens placement for aphakic eyes is ideal, but it is very difficult technique[15].
In previous observations very good results are obtained when the hydrophobic acrylic lenses were implanted[3,16]. AAPOS (American Association for Pediatric Ophthalmology and Strabismus) recommends Single-piece AcrySof lens to implant in children. It is easy to implant and it is safe even in infants and in children with microphthalmia. Hydrophobic acrylic lens implantation is also associated with a lower risk of posterior capsule opacification and secondary glaucoma[3]. On the hydrophilic acrylic lens surfaces deposits of calcium and phosphate in a short period after surgery were observed[17,18]. The silicone lenses also accelerate the development of calcium deposits and are often associated with higher risk of posterior capsular phimosis[19]. Multifocal lenses due to the necessity of precise biometrics and perfect centration, which may change during healing, fibrosis and growth of the eye, are not recommended for implantation in children. In recent years, there are the publications, in which the authors described the use of iris claw IOL in children. Sminia et al implanted Artisan lens in 10 children with mean age 7.4 years in years 1991-1999. Mean corneal endothelial cell density (ECD) was 2702 cells/mm² 12 years after surgery, and was comparable to the mean normal ECD for this age group reported in the literature[20].
Difficulties during cataract surgery in children
Cataract surgery in children is technically more difficult than in adults. This is due to the anatomy of the child eye. The lens is small, anterior chamber is shallow, anterior capsule is very elastic and thick, posterior capsule is 3-5 times thinner and less elastic than in adults. In addition, low scleral rigidity makes it hard to get self-sealing incision. Difficulties with mydriasis often require the use of iris retractors. During surgery an increased vitreous pressure is often observed, usually as a result of scleral subsidence, resulting in shallowing of the anterior chamber and iris prolapse. Due to rising of vitreous pressure, IOL tends to “twisting” from the capsular bag, instead of being placed inside it. In addition, early and late postoperative complications occur more frequently than in adults. Very strong inflammatory reactions, fibrosis and quickly posterior capsule opacification require special intra- and postoperative management.
Surgical technique
The most frequent operational dilemmas in pediatric cataract surgery are: the management with anterior and posterior capsule, and performing of anterior vitrectomy. Operating access is generally through the cornea or the pars plana. Average pars plana width range from 1.5-2 mm in the newborn, to 3 mm at 6 months of age. Manual anterior continuous curvilinear capsulorhexis (ACCC) with the most regular edge is gold standard for the successful outcome of pediatric cataract surgery. It is preferred by surgeons for patients aged 2 years and older. Vitrectorhexis is preferred by surgeons during the first 2 years of life. Anterior capsulotomy can be done using radiofrequency endodiathermy, but the final size will be larger. Posterior capsule opacification (PCO) is the result of proliferation, migration and metaplasis of epithelial cells deriving from the equator region of the anterior capsule to the posterior capsule. When the posterior capsule is left intact during surgery, the incidence PCO is 100%,. Occurrence of PCO increases usually 18 months after surgery. Therefore, in children younger than 8 years posterior capsulotomy should be performed with an additional anterior vitrectomy[21]. Wilson leaves posterior capsule intact in children over 6 years of age. In small children he performs posterior capsulotomy through the pars plana: in infants 0,5 mm posterior to the limbus, under 1 year – 2 mm posterior to the limbus, under 4 year – 2,5 mm posterior to the limbus and in children over 4 years of age – 3 mm posterior to the limbus[3]. When the vitreous body is cut from the back, it is associated with a lower risk of retinal detachment and cystoid macular edema. Posterior capsule management in children with congenital cataract, recommended by Vasavada, is shown in Table II[22].

Complications after surgery
The most common complication described after congenital cataract surgery is secondary glaucoma. Its prevalence is determined on 15.4 -19.5% within 10 years after surgery[1,2]. Therefore, regular medical examinations for many years after surgery are very important. Age less than nine months at the time of surgery and microcornea predispose to development of secondary glaucoma[2]. In children operated before 9 months of age, glaucoma occurs 3.8 times more often than in children operated after this period of life[2,23]. PHPV, primary posterior capsulotomy or anterior vitrectomy does not predispose to development of secondary glaucoma[2]. In patients with glaucoma, bilateral cataract was slightly more common than unilateral lens opacities[2]. The mean time to glaucoma after congenital cataract surgery was ranged from weeks to many years[2,8,23].Retinal detachment in children after congenital cataract surgery has been reported rarely[13]. The less common post-operative complication is fibrinous uveitis[4].
In the available literature reports of increasing myopia in children can be found, especially in the first 2 years after surgery[12,14].
Summary
Success in the treatment of congenital cataract primarily depends on early diagnosis of the disease. The success affects the optimal surgery time, early visual rehabilitation and good cooperation with parents. Fulfilling all these criteria determines a useful visual acuity, which will depend on the functioning in adulthood.
Alina Bakunowicz-?azarczyk, Beata Urban, Anna Bryl
Department of Pediatric Ophthalmology MU in Bialystok, Poland
For any question e-mail: alina.lazarczyk@umb.edu.pl
References
1. Chan WH, Biswas S, Ashworth JL, Lloyd IC. Congenital and infantile cataract: aetiology and management. Eur J Pediatr. 2012 Apr;171(4):625-30.
2. Swamy BN, Billson F, Martin F, Donaldson C, Hing S, Jamieson R, Grigg J, Smith JE. Secondary glaucoma after paediatric cataract surgery. Br J Ophthalmol. 2007 Dec;91(12):1627-30.3. Wilson ME, Pandey SK, Thakur J. Paediatric cataract blindness in the developing world: surgical techniques and intraocular lenses in the new millennium. Br J Ophthalmol 2003;87:14–19
4. Khanna RC, Foster A, Krishnaiah S, Mehta MK, Gogate PM. Visual outcomes of bilateral congenital and developmental cataracts in young children in south India and causes of poor outcome. Indian J Ophthalmol. 2013 Feb;61(2):65-70.
5. Birch EE, Cheng C, Stager DR Jr, Weakley DR Jr, Stager DR Sr. The critical period for surgical treatment of dense congenital bilateral cataracts. 2009 J AAPOS. 2009 Feb;13(1):67-71.
6. Lagrèze WA. The management of cataract in childhood 2009 Klin Monbl Augenheilkd. 2009 Jan;226(1):15-21.
7. Lloyd IC, Ashworth J, Biswas S, Abadi RV. Advances in the management of congenital and infantile cataract. Eye (Lond). 2007 Oct;21(10):1301-9.
8. Lambert SR, Purohit A, Superak HM, Lynn MJ, Beck AD. Long-term Risk of Glaucoma After Congenital Cataract Surgery. Am J Ophthalmol. 2013 Apr 30. pii: S0002-9394(13)00177-3.
9. Enyedi LB, Peterseim MW, Freedman SF, Buckley EG. Refractive changes after pediatric intraocular lens implantation. Am J Ophthalmol. 1998 Dec;126(6):772-81.
10. Andreo LK, Wilson ME, Saunders RA. Predictive value of regression and theoretical IOL formulas in pediatric intraocular lens implantation. J Pediatr Ophthalmol Strabismus. 1997 Jul-Aug;34(4):240-3.
11. Dahan E, Drusedau MU. Choice of lens and dioptric power in pediatric pseudophakia. J Cataract Refract Surg. 1997;23 Suppl 1:618-23.
12. Lu Y, Ji YH, Luo Y, Jiang YX, Wang M, Chen X Graefes Visual results and complications of primary intraocular lens implantation in infants aged 6 to 12 months. Arch Clin Exp Ophthalmol. 2010 May;248(5):681-6.
13. Keech RV, Tongue AC, Scott WE. Complications after surgery for congenital and infantile cataracts. Am J Ophthalmol. 1989 Aug 15;108(2):136-41.
14. O’Keefe M, Fenton S, Lanigan B. Visual outcomes and complications of posterior chamber intraocular lens implantation in the first year of life. J Cataract Refract Surg. 2001 Dec;27(12):2006-11.
15. Peterseim MW, Wilson ME. Bilateral intraocular lens implantation in the pediatric population. Ophthalmology. 2000 Jul;107(7):1261-6.
16. Knight-Nanan D, O’Keefe M, Bowell R. Outcome and complications of intraocular lenses in children with cataract. J Cataract Refract Surg. 1996 Jul-Aug;22(6):730-6.
17. Luo L, Lin H, Chen W, Wang C, Zhang X, Tang X, Liu J, Congdon N, Chen J, Lin Z, Liu Y: In-the-bag intraocular lens placement via secondary capsulorhexis with radiofrequency diathermy in pediatric aphakic eyes. PLoS One. 2013 Apr 24;8(4):e62381
18. Vasavada AR, Raj SM, Shah A, Shah G, Vasavada V, Vasavada V. Comparison of posterior capsule opacification with hydrophobic acrylic and hydrophilic acrylic intraocular lenses. J Cataract Refract Surg. 2011 Jun;37(6):1050-9.
19. Pehere NK, Bojja S, Vemuganti GK, Vaddavalli PK, Samant M, Jalali S, Bhate M. Opacification of intraocular lenses implanted during infancy: a clinicopathologic study of 4 explanted intraocular lenses. Ophthalmology. 2011 Nov;118(11):2128-2132.
20. Kleinmann G, Mamalis N, Apple DJ, Assia EI. Opacification of the Acryl C160 hydrophilic acrylic intraocular lens. J Cataract Refract 2006 Feb;32(2):367-8.
21. Dorey MW, Brownstein S, Hill VE, Mathew B, Botton G, Kertes PJ, El-Defrawy S. Proposed pathogenesis for the delayed postoperative opacification of the hydroview hydrogel intraocular lens. Am J Ophthalmol. 2003 May;135(5):591-8.
22. Sminia ML, Odenthal MT, Prick LJ, Mourits MP, Völker-Dieben HJ. Long-term follow-up of the corneal endothelium after aphakic iris-fixated IOL implantation for bilateral cataract in children. J Cataract Refract Surg. 2011 May;37(5):866-72.
23. Dahan E, Salmenson BD. Pseudophakia in children: precautions, technique, and feasibility. J Cataract Refract Surg. 1990 Jan;16(1):75-82.
24. Vasavada AR, Praveen MR, Tassignon MJ, Shah SK, Vasavada VA, Van Looveren J, De Veuster I, Trivedi RH. Posterior capsule management in congenital cataract surgery. J Cataract Refract Surg 2011 J Cataract Refract Surg. 2011.
25. B. Urban, A. Bakunowicz-?azarczyk: Aphakic glaucoma after pediatric cataract surgery with and without intraocular lens implantation. Klin. Oczna 2010,112(4-6):105-107.
Dr. Carmelo Chines
Direttore responsabile
