Varie condizioni degenerative possono interessare il corpo vitreo e la retina, anche se l’intima funzione di queste due strutture crea spesso difficoltà a determinare quale tessuto sia stato interessato per primo nel processo patologico.
Con il termine di “degenerazioni vitreo-retiniche” sono raggruppate quelle situazioni patologiche in cui le alterazioni coinvolgono entrambe le strutture.
Le degenerazioni vitreo-retiniche possono essere di origine ereditaria “vitreoretinopatie ereditarie” (Tab. I) o acquisite “ialoidoretinopatie”.
Queste ultime (Tab. II) possono essere sia legate all’invecchiamento del vitreo (sineresi vitreale e distacco del vitreo), sia secondarie alla presenza di depositi extracellulari, proteici (amiloidosi vitreale) o lipidici (vitreopatiaasteroide e sinchisi scintillante).
Nel presente capitolo vengono discusse tre condizioni cliniche comunemente indicate con il termine di vitreopatie degenerative:
Il termine di vitreopatie degenerative è tuttavia improprio (1) dal momento che implica un processo primario a livello del gel vitreale, mentre l’unica degenerazione primaria del vitreo è rappresentata dalla sineresi e dal distacco di vitreo, mentre la maggior parte delle vitreopatie degenerative sono secondarie a degenerazioni retiniche ed il materiale che si accumula nel vitreo proviene da strutture diverse da esso, anche se questo non è ancora stato dimostrato in maniera definitiva nel caso della vitreopatia asteroide.
VITREOPATIA ASTEROIDE
La degenerazione asteroide del vitreo è stata descritta per la prima volta da Schmidt (2) ed è stata differenziata dalla sinchisi scintillante da Benson nel 1894 (3). Nella letteratura europea si possono ancora incontrare le varianti proposte da Wiegmann (4): “Scintillatio nivea” e “scintillatio albescens”.
La vitreopatia asteroide è un’affezione rara, con una prevalenza nella popolazione generale tra 0.15% e 0.9% (5).
Unilaterale nel 75% dei casi, si riscontra generalmente nei soggetti d’età superiore ai 60 anni ed è più frequente nei diabetici.
Clinica. L’aspetto caratteristico della vitreopatia asteroide è rappresentato dalla presenza di opacità rotonde bianco-giallastre e brillanti, sospese nel gel vitreale (Fig. 1), spesso aggregate in ammassi e dall’aspetto simile a fili o grappoli di perle.
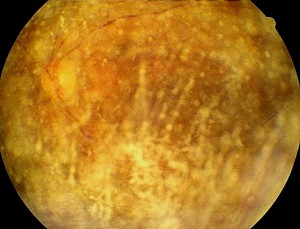
Il vitreo presenta un aspetto normale: la liquefazione vitreale ed il DPV sono presenti solo nel 12% dei soggetti (6). I corpi asteroidi sono attaccati alle fibre del collageno e sono mobili con i movimenti del gel vitreale. All’esame ecografico si osserva una moltitudine di picchi iperecogeni, mobili con il movimento del bulbo oculare. Una caratteristica costante è la presenza di una corona vitreale ipoecogena tra l’immagine iper-riflettente dei corpi asteroidi e la superficie anteriore della retina, che può essere confusa con un distacco posteriore del vitreo.
La vitreopatia asteroide è generalmente asintomatica. Anche se le opacità sono talmente dense da ostacolare la visione del fondo oculare, i pazienti non hanno una riduzione dell’acuità visiva e la malattia rappresenta spesso una scoperta fortuita durante un esame oculistico di routine.
Quando è presente una notevole diminuzione visiva, bisogna sospettare una patologia retinica associata (degenerazione maculare legata all’età, retinopatia diabetica, ecc.).
Istopatologia. L’analisi al microscopio elettronico a trasmissione ha evidenziato la presenza di lipidi complessi e l’analisi a diffrazione di raggi X ha mostrato che le particelle asteroidi sono formate dall’apposizione di strati concentrici di fosfolipidi associati a complessi calcio-fosfato, intimamente legati al collageno vitreale (6).
Eziologia. L’eziologia resta ancora sconosciuta.
Non sono state dimostrate associazioni con altre condizioni patologiche oculari o sistemiche (7): il legame con il diabete mellito, riportato in alcuni studi iniziali (8), è stato successivamente messo in dubbio per carenze metodologiche nelle ricerche effettuate (9).
Nessuno studio, inoltre, ha riportato l’associazione di ialopatia asteroide con una dislipidosi ereditaria.
Trattamento. La degenerazione asteroide richiede raramente un trattamento terapeutico perché è di solito asintomatica e scevra di complicanze (10).
Nei rari casi in cui è presente una massiva concentrazione di corpi asteroidi nella parte centrale della cavità vitreale, può verificarsi una discreta diminuzione visiva.
Una scarsa visibilità del fondo oculare non consente, talvolta, la sorveglianza di una patologia del segmento posteriore e l’eventuale realizzazione di una fotocoagulazione retinica. In questi casi può essere proposta una vitrectomia via pars plana (10-14) (Fig. 2).

Tuttavia la vitrectomia nella degenerazione asteroide non è esente da rischi (1, 11, 15) e potrebbe addirittura favorire un distacco di retina postoperatorio. Questa complicanza si verifica probabilmente perché in questa patologia il distacco posteriore di vitreo e la liquefazione vitreale sono significativamente meno frequenti rispetto alla popolazione normale d’età analoga (p<0.01), mentre l’aderenza vitreoretinica è maggiore (1).
SINCHISI SCINTILLANTE
La sinchisi scintillante è una condizione degenerativa del vitreo spesso confusa con la vitreopatia asteroide, dalla quale deve essere differenziata sia sul piano clinico che su quello patologico.
Clinica. Descritta per la prima volta da Sichel nel 1846 (16), si presenta clinicamente con minute multiple particelle cristalliniche, brillanti e colorate, sospese in un vitreo degenerato e liquefatto (17).
L’aspetto di questi corpuscoli è piatto ed angolare, contrariamente a quello rotondeggiante dei corpi asteroidi.
I cristalli sono mobili con i movimenti dell’occhio, ma indipendenti dai movimenti del vitreo, a differenza dei corpi asteroidi che sono strutturalmente associati al vitreo.
Durante i movimenti oculari si diffondono rapidamente nella cavità vitrea come coriandoli multicolori, ma si depositano per gravità sul fondo oculare, quando l’occhio è immobile.
Nei pazienti fachici le particelle possono accumularsi in camera anteriore (Fig. 3) e simulare un ipopion (18, 19). Talvolta si può sviluppare un glaucoma secondario (18, 19).
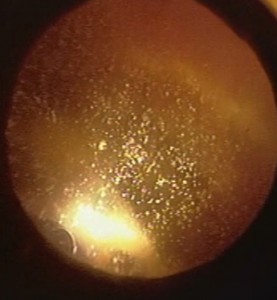
L’aspetto ecografico corrisponde ad una moltitudine di punti mediamente ecogeni.
La sinchisi scintillante viene riscontrata più spesso in soggetti al di sotto dei 35 anni di età (20), mentre la ialoidopatia asteroide si manifesta negli anziani.
La sinchisi scintillante si presenta esclusivamente in occhi gravemente traumatizzati o affetti da infiammazioni croniche (17) o in seguito ad emorragie intravitreali (21).
Istopatologia. Gli studi istopatologici hanno ulteriormente differenziato la sinchisi scintillante dalla vitreopatia asteroide. I cristalli della sinchisi, infatti, sono costituiti da cristalli di colesterolo, mentre i corpi asteroidi risultano composti da un complesso calcio-fosfolipidico (22). Per questo motivo il termine più appropriato per quest’affezione sarebbe “cholesterosis bulbi”.
Eziologia. L’esatta eziologia dei cristalli di colesterolo non è chiara. Con ogni probabilità il colesterolo deriva dalla distruzione cellulare di globuli rossi o leucociti lisati provenienti da emovitreo o flogosi cronica (22).
Trattamento. La presenza di cristalli di colesterolo in camera vitrea non richiede alcun trattamento; tuttavia i pazienti afachici con quest’affezione possono sviluppare un glaucoma, quando le particelle ostruiscono l’angolo di filtrazione. In questi casi è utile praticare una vitrectomia ed un lavaggio della camera anteriore.
AMILOIDOSI VITREALE
L’amiloidosi è una patologia caratterizzata dalla deposizione extracellulare di una sostanza proteica anomala che presenta caratteristiche tintoriali, biochimiche e ultrastrutturali particolari. La proteina anomala è una prealbumina, dipendente da una mutazione a livello della transtiretina.
La patogenesi di questa complessa malattia rimane oscura.
La classificazione anatomo-patologica attuale distingue le amiloidosi in sistemiche (poliviscerali) o localizzate (monoviscerali), primarie o secondarie, familiari o idiopatiche (23).
Le localizzazioni oculari sono multiple e possono interessare i muscoli oculo-motori, la ghiandola lacrimale, le palpebre, le congiuntive, la cornea, il vitreo, la retina e l’orbita.
Nonostante l’amiloidosi come malattia a sé stante sia stata riconosciuta già agli inizi del XIX secolo, l’interessamento vitreale è stato osservato solo nel 1953 (24).
Clinica. Le alterazioni del vitreo si repertano essenzialmente nelle neuropatie amiloidi eredofamiliari tipo I e II e possono rappresentare la prima manifestazione della malattia, insorgendo molto tempo prima del coinvolgimento di altri organi.
Si presentano clinicamente (23, 25, 26, 27) come depositi biancastri a contatto dei vasi retinici, in particolar modo attorno alle arteriole, simulando l’aspetto di un essudato cotonoso.
La densità dei depositi d’amiloide aumenta progressivamente giungendo a coprire interi tratti di vasi retinici. Le opacità si estendono successivamente nella cavità vitreale formando aggregati granulari con bordi lievemente sfrangiati che si diffondono in senso postero-anteriore e s’inseriscono alla faccia posteriore del cristallino sotto forma d’opacità biancastre con pseudopodi, assumendo l’aspetto di “veli di merletto” o di “lana di vetro”. Questo aspetto, bilaterale e simmetrico, è specifico della malattia.
L’amiloidosi vitreale è spesso asintomatica. Una diminuzione visiva si verifica quando le opacità vitreali sono dense o si accumulano a livello della capsula posteriore del cristallino.
Raramente è associata a complicanze, tuttavia la sostanza amiloide può strozzare e obliterare i vasi coroideali e/o retinici e comportare neovascolarizzazione retinica periferica ed emorragie vitreali (28).
Nella forma evolutiva si può sviluppare un glaucoma ad angolo aperto secondario alla presenza di depositi amiloidi nel trabecolato. Un glaucoma secondario può insorgere anche per un aumento della pressione venosa episclerale in caso di lesione amiloide delle vene episclerali (29).
Trattamento. L’unica forma di trattamento dell’amiloidosi vitreale è la vitrectomia via pars plana (26, 30-33). L’intervento è indicato, quando le opacità vitreali provocano una significativa riduzione visiva.
La vitrectomia deve essere completa e soprattutto retrolentale, perché le recidive sono generalmente dovute alla permanenza di vitreo dietro il cristallino.
Se è presente un distacco posteriore del vitreo la prognosi è favorevole. Se invece il vitreo non è distaccato, esiste il rischio di provocare emorragie e rotture retiniche iatrogene e di non poter rimuovere le opacità amiloidi saldamente aderenti alla retina.
Prof. Raffaello di Lauro,
Dott.ssa Maria Teresa di Lauro,
Dott.ssa Raffaella di Lauro,
Dott. Alessandro Senese,
Dott.ssa Paola Giustiniani,
Dott.ssa Antonietta D’Aloia
Divisione Oculistica del CTO – NAPOLI
BIBLIOGRAFIA
1) Schepens C.L., Neetens A. “The vitreous and vitreoretinal disorders”. Springer-Verlag Ed., Ny, 1990, 109-127.
2) Schmidt: cit da Wiegmann.
3) Benson A.H. “Diseases of the vitreous. A case of mononuclear asteroid hyalitis”. Trans. Ophthalmol. Soc. Uk, 1894, 14: 101-104.
4) Wiegmann “Ein beitrag zur genese und zum bilde der synchisis scintillans“. Klin. Mon. Augen, 1918, 61:82-88.
5) Safir A. et al. “Is asteroid hyalosis ocular gout?” Ann. Ophthalmol. , 1990, 22: 70-77.
6) Topilow H. Et Al. “Asteroid hyalosis. biomicroscopy. Ultrastructure and composition”. Arch. Ophthalmol. 1982, 100: 964-968.
7) Bergren R.L., Brown G.C., Duker J.S. “Prevalence and association of asteroid hyalosis with systemic disease”. Am. J. Ophthalmol., 1991, 11: 289-293.
8) Smith J.L. “Asteroid hyalitis: incidence of diabetes mellitus and hypercholesterolemia”. J.A.M.A., 1958, 168: 891-893.
9) Luxenberg M., Sime D. “Relationship of asteroid hyalosis to diabetes mellitus and plasma lipids levels”. Am. J. Ophthalmol., 1969, 67: 406-413.
10) Feist R.M. Et Al. “Vitrectomy in asteroid hyalosis”. Retina, 1990, 10: 173-177.
11) Parnes R.E., Zakov Z.N., Ovak M.A., Rice J.A. “Vitrectomy in patients with decreased visual acuity secondary to asteroid hyalosis”. Am. J. Ophthalmol., 1998, 125: 703-704.
12) Lambrov F.H.Jr Et Al. “Vitrectomy when asteroid hyalosis prevents laser photocoagulation”. Ophthalmic Surg., 1989, 20: 100-102.
13) Olea Vallejo Et Al. “Vitrectomy for asteroid hyalosis”. Arch. Soc. Esp. Oftalmol., 2002, 77: 201-204.
14) Boissonnot M., Manic H., Balayre S., Dighero P. “Indications de la vitrectomie chez les patients atteints d’une baisse d’acuite visuelle secondarie a une hyalopatie asteroide”. J. Fr. Ophtalmol., 2004, 7: 791-794.
15) Ikeda T. Et Al. “Vitrectomy for proliferative diabetic retinopathy with asteroid hyalosis”. Retina, 1998, 18: 410-414.
16) Sichel J. “Note Complementaire Sur Le Synchisis Etincellent”. Ann. Oculist., 1846, 15: 248.
17) Wand M., Smith T.R., Cogan D.G. “Cholesterosis bulbi: the ocular abnormality knows as synchisis scintillans”. Am. J. Ophthalmol., 1975, 80: 177-183.
18) Michiels J., Garin P. “Synchisis scintillans of the anterior chamber”. Bull. Soc. Belge Ophtalmol., 1969, 152: 455-458.
19) Eke T., Richer R.G. “Pseudohypopyon to synchisis scintillans”. Eye, 1996, 10: 527-528.
20) Hogan M.J., Zimmerman L.E. “Ophthalmic pathology”. 2nd Ed. Sauders, Philadelphia, 1962, 650-654.
21) Spraul C.W., Grossniklaus H.E. “Vitreous haemorrhage”. Surv. Ophthalmol., 1997, 42: 3-39
22) Andrews J.S., Lynn C., Scobey J.W., Elliot J.H. “Cholesterosis bulbi. Case report with modern chemical identification of the ubiquitous crystals”. Br. J. Ophthalmol., 1973, 57: 838-844.
23) Flament J., Storck D. “Oeil Et Pathologie Generale”. Masson Ed., Paris, 1997, 176-179.
24) Kantarjian A.D., Dejong R.N. “Familial primary amyloidosis with nervous system involvement”. Neurology, 1953, 3: 399-409.
25) Dhermy P. “Amylose oculaire”. J. Fr. Ophtalmol., 1987, 10: 91-103.
26) Doft B.M., Machemer R. et al. “Pars plana vitrectomy for vitreous amyloidosis”. Am. J. Ophthalmol., 1970, 94: 982-991.
27) Monteiro G.J., Martins A.F. et al. “Ocular changes in familial amyloidotic polyneuropathy with dense vitreous opacities”. Eye, 1991, 5: 99-105.
28) Savage D.J., Mango C.A. “Amyloidosis of the vitreous. fluorescein angiographic findings and neovascularization”. Arch. Ophthalmol., 1982, 100: 1776-1779.
29) Nelson G.A., Edward D.P., Wilensky J.T. “Ocular amyloidoses and secondary glaucoma”. Ophthalmology, 1999, 106: 1363-1366.
30) Treister G., Gad K. “Treatment of vitreous opacities in a case of familial amyloidotic polyneuropathy by vitreous surgery”. Metab. Paediatric. Ophthalmol., 1981, 5: 105-108.
31) Irvine A.R., Char D.H. “Recurrent amyloid involvement in the vitreous body after vitrectomy”. Am. J. Ophthalmol., 1976, 82: 705-708.
32) Sandgren O., Stenkula S., Dedorson I. “Vitreous surgery in patients with primary neuropathic amyloidosis”. Acta Ophthalmol., 1985, 63: 383-388.
33) Gastaud P., Betis F. “Modifications degenerative du vitre” in “Brasseur G.: Pathologie Du Vitre”. Masson Ed. Paris, 2003, 149-155.
Dr. Carmelo Chines
Direttore responsabile